诊所常用医疗器械电磁兼容性检测
服务地区:全国
报告类型:电子报告、纸质报告
取样方式:快递邮寄或上门取样
报告语言:中文报告、英文报告、中英文报告
样品要求:样品数量及规格等视检测项而定
注:因业务调整,微析暂不接受个人委托测试。
北京微析技术研究院进行的相关[诊所常用医疗器械电磁兼容性检测],可出具严谨、合法、合规的第三方检测报告。
如果您对[诊所常用医疗器械电磁兼容性检测]有报告、报价、方案等问题可咨询在线工程师,收到信息会在第一时间联系您...
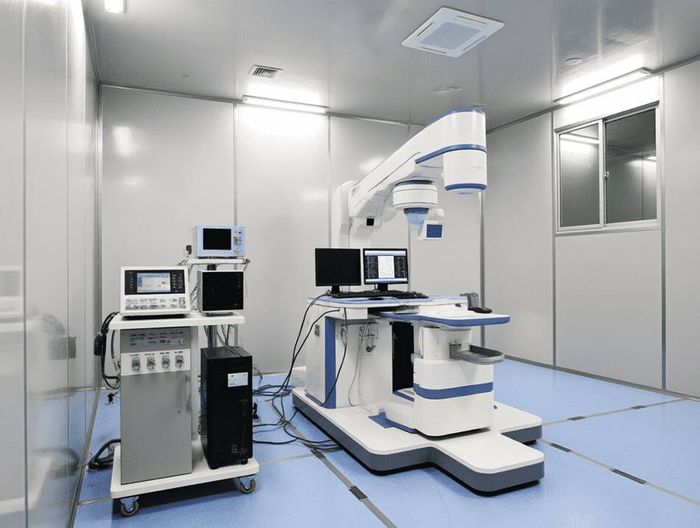
诊所常用医疗器械电磁兼容性(EMC)检测是确保设备在电磁环境中安全运行的关键环节,涵盖辐射发射、抗扰度等核心测试项目。该检测依据YY 9706.102-2021、GB 4824等标准,验证心电图机、输液泵等设备在诊所复杂电磁环境下不干扰其他设备且自身功能不受影响。通过系统性测试,可有效降低医疗事故风险,保障患者安全和诊疗质量。
诊所常用医疗器械电磁兼容性检测项目介绍
该项目针对诊所环境中的有源医疗器械,评估其在电磁环境中的兼容能力。核心测试包括辐射发射(验证设备是否产生过量电磁干扰)、传导发射(检测通过电源线传播的干扰)以及静电放电、射频辐射抗扰度等抗干扰能力验证。
测试依据强制性行业标准YY 9706.102-2021《医用电气设备 第1-2部分:安全通用要求 并列标准:电磁兼容》展开,同时参考GB/T 18268.1等通用标准。典型检测对象涵盖监护仪、雾化器、高频电刀等诊所常规设备。
检测重点关注设备在典型工作模式下的电磁特性,如心电图机在信号采集、数据传输等不同状态下的EMC表现。通过模拟诊所真实电磁环境(包括Wi-Fi、蓝牙等无线信号干扰),评估设备共址工作时的相互影响。
诊所常用医疗器械电磁兼容性检测范围
覆盖诊所内所有带电子控制单元的二类、三类医疗器械,包括但不限于:电动手术床、超声雾化器、自动体外除颤器(AED)、电子血压计等。特别关注具有无线通信功能的设备,如远程监护系统的蓝牙模块。
检测频段覆盖150kHz-6GHz,模拟从工频谐波到5G通信的全频谱干扰环境。对于含金属外壳的大型设备(如DR数字成像系统),需额外评估屏蔽效能对检测结果的影响。
检测场景包含设备单独工作、多设备并行运行以及突发干扰(如除颤器放电)等复合工况。特别规定设备在最大功率输出、最低供电电压等极限状态下的EMC表现。
诊所常用医疗器械电磁兼容性检测所需样品
需提供完整成品设备,包含标准配置的电源适配器、数据线等附件。对于多模块设备(如中心监护系统),要求主机与各分机组成完整系统送检。
样品应处于典型工作状态,如输液泵需配备模拟负载液袋,高频电刀需连接标准负载电阻。要求提供设备所有可调节的工作模式说明,包括最大/最小功率设置、通信频段切换等功能。
特殊情况下需提供专用测试夹具,如内窥镜的弯曲状态模拟装置。对植入式设备(如临时起搏器),需提供人体组织等效模拟液等配套测试环境。
诊所常用医疗器械电磁兼容性检测所需设备
核心设备包括3米法半电波暗室(满足CISPR 16-1-4要求)、EMI接收机(频率范围覆盖9kHz-18GHz)、静电放电模拟器(接触放电±8kV,空气放电±15kV)。
抗扰度测试需射频场强产生系统(80MHz-6GHz,场强可达30V/m)、工频磁场发生器(50Hz,100A/m)。传导测试配备LISN网络(V型与Δ型)、电流探头(频率至100MHz)。
辅助设备包含转台(360°连续旋转)、升降天线塔(1-4m可调)、屏蔽室(背景噪声≤6dBμV)。数据采集系统需满足CISPR 16-2-1规定的检波方式和扫描速度。
诊所常用医疗器械电磁兼容性检测流程
第一阶段进行设备预扫描,在开放测试场地使用频谱分析仪快速定位干扰源。第二阶段在电波暗室开展符合性测试,按照GB 4824分类确定限值要求。
抗扰度测试采用逐级递增法,从标准规定强度的70%开始施加干扰,观察设备性能降级情况。对于生命支持类设备(如呼吸机),需在测试中持续监测关键参数。
数据记录需包含设备在所有测试方位的辐射最大值,采用峰值、准峰值、平均值检波器同步测量。最终报告需明确整改建议,如滤波器参数调整、接地优化方案等。
诊所常用医疗器械电磁兼容性检测技术与方法
辐射发射测试采用替代法测量,使用宽带喇叭天线(1-18GHz)结合对数周期天线(30MHz-1GHz)。测试距离严格控制在3米,高度扫描范围1-4米。
传导骚扰测试使用V型人工电源网络,在相线、中线分别测量150kHz-30MHz频段骚扰电压。对于直流供电设备,采用电流探头法测量电源端骚扰电流。
静电放电测试依据IEC 61000-4-2,对设备金属外壳、显示屏、连接器等易接触部位施加±4kV~±15kV放电。射频场感应的传导骚扰测试使用CDN耦合装置,频率范围150kHz-80MHz。
诊所常用医疗器械电磁兼容性检测标准与规范
GB 4824-2019《工业、科学和医疗设备 射频骚扰特性 限值和测量方法》:划分Group1(非射频设备)与Group2(含射频能量设备)的限值要求。
YY 9706.102-2021:明确医用设备抗扰度测试等级,规定生命支持设备在射频电磁场30V/m强度下不得出现性能降级。
GB/T 17626系列(等同IEC 61000-4):包含静电放电(第2部分)、射频场辐射抗扰度(第3部分)、电快速瞬变脉冲群(第4部分)等具体测试方法。
CISPR 11:2015:针对ISM设备的射频骚扰测量,规定6dB带宽测量法及现场测量替代方案。
IEC 60601-1-2:2014:医疗电气设备EMC通用标准,要求设备在测试期间维持基本性能。
GB/T 18268.1-2019:实验室设备EMC要求,适用于诊所检验科设备。
YY 0505-2012:医用电气设备EMC专用要求,规定抗扰度测试的性能判据等级。
ISO 13485:2016:医疗器械质量管理体系,要求建立EMC设计验证流程。
FDA指南文档:针对出口美国的设备,需满足21 CFR Part 18的辐射发射限值。
欧盟RED指令(2014/53/EU):涉及无线医疗设备的射频参数测试要求。
诊所常用医疗器械电磁兼容性检测服务周期
常规检测周期为5-7个工作日,包含预测试、正式测试、数据分析等环节。复杂系统(如含多频段无线模块的设备)检测需延长至10-15个工作日。
加急服务可在3个工作日内完成基础项目测试,但需支付30%加急费用。整改复测周期通常为3-5个工作日,包含问题定位、方案实施和验证测试。
年度监督检测采用简化程序,周期缩短至2-3个工作日,主要验证关键参数是否符合既往报告数据。
诊所常用医疗器械电磁兼容性检测应用场景
新产品注册检测:依据《医疗器械注册管理办法》要求,二类、三类有源器械必须通过EMC检测方可上市。
设备安装验收:诊所引进大型设备(如CT)时,需验证其与现有设备的电磁兼容性。
定期维护检测:根据YY/T 0466.1标准,建议每24个月对生命支持类设备进行EMC复检。
医疗事故溯源:当出现设备异常关机、数据错误时,EMC检测可排查电磁干扰因素。
设备改造验证:涉及电路修改、外壳材质变更或新增无线功能时,需重新进行EMC评估。