眼科手术器械生物相容性检测
服务地区:全国
报告类型:电子报告、纸质报告
取样方式:快递邮寄或上门取样
报告语言:中文报告、英文报告、中英文报告
样品要求:样品数量及规格等视检测项而定
注:因业务调整,微析暂不接受个人委托测试。
北京微析技术研究院进行的相关[眼科手术器械生物相容性检测],可出具严谨、合法、合规的第三方检测报告。
如果您对[眼科手术器械生物相容性检测]有报告、报价、方案等问题可咨询在线工程师,收到信息会在第一时间联系您...
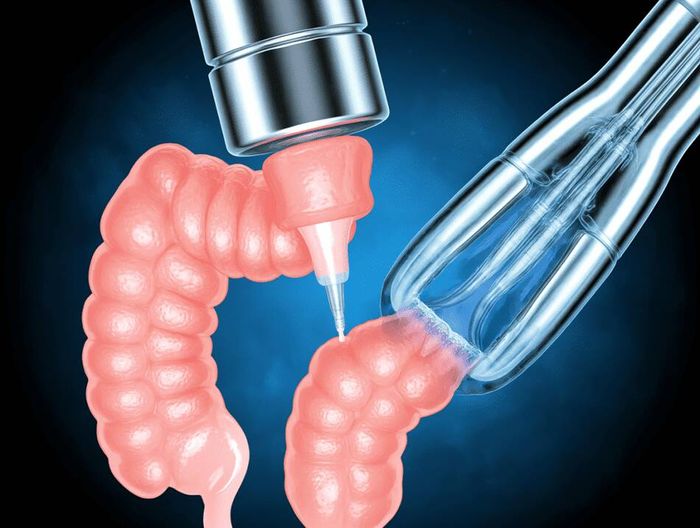
眼科手术器械生物相容性检测是确保器械与人体组织接触时无毒性、无致敏性的关键质量控制环节。该检测依据ISO 10993系列标准,涵盖细胞毒性、刺激反应、遗传毒性等10余项测试,重点评估器械材料在角膜、晶状体等敏感眼部组织的生物安全性。检测需模拟器械实际使用环境,通过体外实验、动物实验双重验证,为眼科高精度手术器械(如超声乳化手柄、人工晶体植入器等)上市提供法定合规依据。
眼科手术器械生物相容性检测项目介绍
该检测针对接触眼表及眼内组织的器械,包含材料溶出物分析、细胞毒性测试等基础项目。例如超声乳化手术中使用的钛合金穿刺刀需进行持续21天的植入物刺激试验,检测金属离子释放对虹膜组织的影响。对于含有药物涂层的青光眼引流阀,需额外开展亚慢性毒性研究和局部植入反应评估。
项目设计需考虑器械与房水、玻璃体等特殊体液的长期接触特性,如人工晶体需进行光老化后的溶出物测试。检测方案需结合器械预期接触时间(短期/持久)制定差异化测试组合,角膜缝合线需完成28天降解产物的系统毒性评估。
眼科手术器械生物相容性检测范围
覆盖三大类器械:1)切割类(超声乳化刀、玻璃体切割头)需检测金属磨损颗粒的生物反应;2)植入物(人工晶体、巩膜扣带)须完成12周兔眼植入实验;3)辅助器械(开睑器、角膜标记环)重点评估重复灭菌后的材料稳定性。特别包含微创器械如25G玻璃体切割头的纳米级碎屑检测,要求达到ISO 10993-17规定的可耐受暴露极限。
眼科手术器械生物相容性检测所需样品
需提供三类样本:1)终产品3件(如完整的人工晶体植入系统);2)同批次材料样本(5×5cm²)用于溶出物检测;3)灭菌后样品(环氧乙烷灭菌需提供解析完成品)。特殊要求包括:角膜接触器械需提供边缘抛光样本,弹性体材料(如硅胶环扎带)需包含硫化前后对比样。
眼科手术器械生物相容性检测所需设备
关键设备包括:1)动态机械分析仪(DMA)检测材料在37℃房水环境下的形变特性;2)电感耦合等离子体质谱仪(ICP-MS)分析金属器械的钴、镍等离子释放量;3)共聚焦显微镜观察细胞在微沟槽器械表面(如多焦点人工晶体)的黏附形态。另需专用眼模型装置模拟前房压力下的器械性能变化。
眼科手术器械生物相容性检测流程
标准流程包含五个阶段:1)材料表征(FTIR分析聚合物器械的化学组成);2)体外实验(角膜上皮细胞培养评估器械浸提液毒性);3)有限元模拟(计算器械-组织界面应力分布);4)动物实验(新西兰兔眼植入6个月观察异物反应);5)临床数据回溯(已有CE认证产品需补充真实世界安全性数据)。
眼科手术器械生物相容性检测技术与方法
核心方法包括:1)MTT比色法量化器械浸提液对角膜内皮细胞增殖的影响;2)反向离子电渗技术检测硅油填充器械的离子渗透性;3)微流控芯片模拟前房环境评估器械表面蛋白吸附量。创新技术如器官芯片(Eye-on-a-chip)已用于评估青光眼引流阀在动态房水循环中的生物相容性。
眼科手术器械生物相容性检测标准与规范
1)ISO 10993-5:2009 细胞毒性试验(ELISA法检测IL-6炎症因子释放量) 2)ISO 11979-5:2020 人工晶状体专用生物相容性要求(包含后囊混浊抑制率测试) 3)GB/T 16886.10-2017 刺激与致敏试验(兔眼结膜囊重复接触试验) 4)USP <87> 体外细胞毒性定性评估(适用于胶原蛋白止血海绵) 5)YY/T 0771.3-2020 眼科激光设备生物安全性(包含光热效应测试) 6)ISO 22442-3:2020 动物源材料病毒灭活验证(适用于羊膜移植器械) 7)ASTM F756-17 材料溶血性标准(评估巩膜缝合线血液相容性) 8)EN ISO 14971:2019 风险管理应用(包含生物相容性风险矩阵分析) 9)CFDA 2018年眼科器械生物学评价指导原则(特殊要求角膜接触器械需进行神经毒性测试) 10)ISO 18562-3:2017 气体通路生物相容性(适用于玻璃体切割系统的气液交换装置)
眼科手术器械生物相容性检测服务周期
常规检测周期为8-16周:体外实验(细胞毒性、致敏性)需2-4周;亚急性毒性实验(28天小鼠植入)需6周;特殊项目如人工晶体钙化沉积测试(加速老化90天)需延长至18周。加急服务可压缩至6周,但需配合提供材料DSC热分析图谱等预检数据。
眼科手术器械生物相容性检测应用场景
主要应用于:1)创新型折叠式人工晶体上市前验证;2)传统不锈钢器械升级为钛合金的生物安全性对比;3)微创青光眼手术(MIGS)器械的长期安全性追踪。典型案例包括:飞秒激光角膜刀涂层脱落风险评估、硅油填充管表面改性后的补体激活测试等。